هل سمعت من قبل عن "خريطة الكيمياء"؟
الجدول الدوري "periodic table"، يُعتبر ترتيب منظم ومتسلسل للعناصر الكيميائية التي تم اكتشافها حتى يومنا هذا؛ لذلك أجد أنه يستحق أن يطلق عليه لقب خريطة الكيمياء. يعد الجدول الدوري مفتاحاً لفهم 118 عنصراً تم اكتشافهم حتى يومنا هذا منذ أن وضع أسسه العالم الروسي ديميتري مندليف في القرن التاسع عشر لذلك يُسمى ب "جدول مندليف".
مكونات الجدول الدوري: المجموعات والدورات
يتكون الجدول الدوري من مجموعات ودورات، فالمجموعات هي الأعمدة الرأسية، والدورات هي الصفوف الأفقية. تتشابه عناصر المجموعة الواحدة في الخواص الفيزيائية والكيميائية، وهذا هو الأساس الذي تم بناء الجدول الدوري عليه.
-
يحتوي الجدول على 18 عموداً رأسياً تُسمى بالمجموعات وتتميز عناصر المجموعة الواحدة بالتشابه في الخصائص الفيزيائية والكيميائية، وذلك بسبب أنها تحمل نفس عدد الإلكترونات في مستوى الطاقة الخارجي للذرة والذي نعبر عنه برقم المجموعة.
-
يتواجد 8 مجموعات رئيسية، و8 مجموعات فرعية. وتم اعتماد الأرقام العربية في ترقيمهم (1,2,3,...) يتبع الترقيم بالحرف A إذا كانت المجموعة رئيسية والحرف B إذا كانت المجموعة فرعية. سنتعرف فيما بعد عن المجموعات الرئيسية والفرعية.
-
يحتوي الجدول على 7 صفوف أفقية تُسمى بالدورات، ويعبر رقم الدورة عن أعلى مستوى من الطاقة ممتلئ بالإلكترونات.
تصنيف العناصر الكيميائية في الجدول الدوري
يتم تصنيف العناصر في الجدول الدوري بناءً على الزيادة في الأعداد الذرية، فتزداد من اليسار إلى اليمين ومن الأعلى إلى الأسفل. بحيث يكون لكل عنصر عدد ذري مساوٍ لعدد البروتونات الموجودة في نواة هذا العنصر.
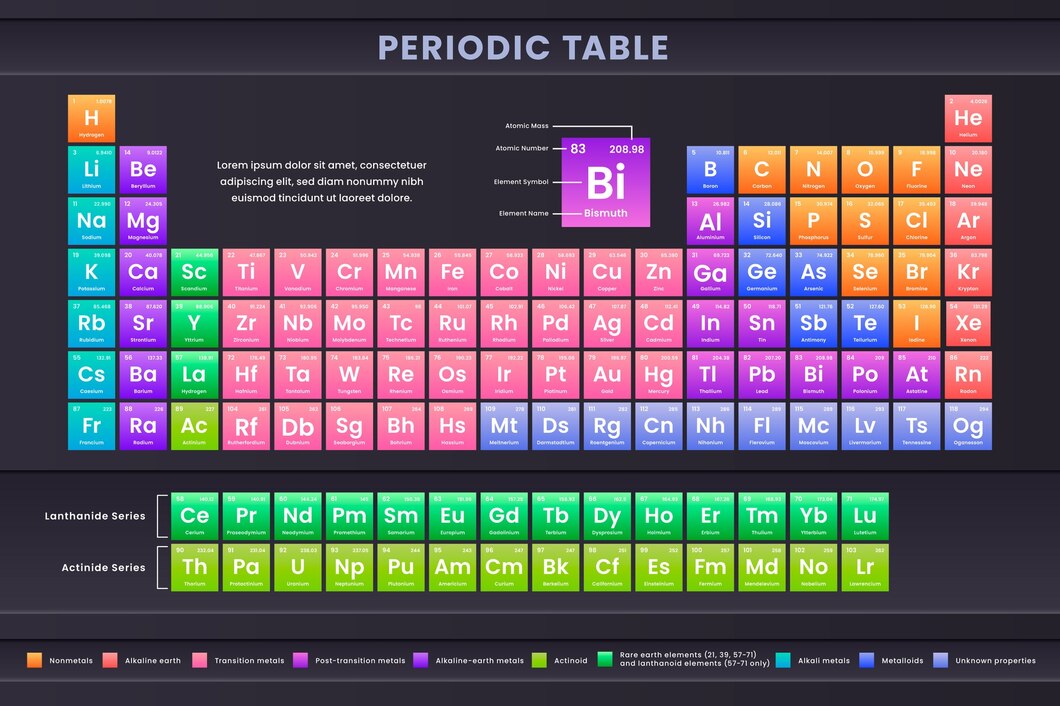
يتم التعبير عن كل عنصر بمربع يحتوي على ما يلي:
-
رمز العنصر "Chemical symbol": والذي قد يكون اختصاراً للعنصر باللغة الانجليزية أو اللاتينية.
-
اسم العنصر: يتواجد اسم كل عنصر أسفل الرمز كاملاً باللغة الإنجليزية.
-
العدد الذري للعنصر "Atomic number": يساوي عدد البروتونات في نواة كل عنصر في الجدول.
-
العدد الكتلي "Atomic mass": يساوي مجموع عدد البروتونات والنيوترونات في نواة كل عنصر في الجدول.
كيف تم تصنيف العناصر في الجدول الدوري؟
تم تصنيف العناصر في الجدول الدوري إلى:
-
فلزات: هي العناصر التي تميل لفقد الإلكترونات لتكوين أيونات موجبة، وتتواجد في يسار ومنتصف الجدول. و تتميز بلمعانها وقدرتها الجيدة على التوصيل للكهرباء والحرارة.
-
لا فلزات: هي العناصر التي تميل لكسب الإلكترونات لتكوين أيونات سالبة، وتتواجد في أعلى يمين الجدول، وهي عناصر غير لامعة وغير موصلة للكهرباء والحرارة.
-
أشباه فلزات: ولها خصائص متوسطة بين الفلزات واللافلزات، تفصل ما بين الفلزات واللافلزات بشكل سُلّمي لأن خواصها تقع ما بين خواص الفلزات و خواص اللافلزات.
المجموعات الثمانية الرئيسية الموجودة في الجدول الدوري وأهم خصائصها:
-
"الفلزات القلوية" (1A): وهي سلسلة العناصر الكيميائية الموجودة في المجموعة الأولى ما عدا الهيدروجين، والتي تبدأ من أقصى يسار الجدول. تتميز عناصر هذه المجموعة بميولها الشديد لفقد الإلكترونات لتكوين أيونات موجبة لذلك فهي عوامل مختزلة قوية، بالإضافة إلى تفاعلها القوي مع الماء، وفقدانها بريقها عند التعرض للهواء. سُميت بالفلزات القلوية لأنها تشكل محاليل قلوية قوية عند تفاعلها مع الماء.
-
"الفلزات القلوية الترابية" (2A): وهي سلسلة العناصر الكيميائية الموجودة في المجموعة الثانية في الجدول. وتتميز هذه العناصر بأنها أكثر صلابة من عناصر المجموعة الأولى، وتكون أيونات ثنائية موجبة الشحنة. سُميت بالفلزات القلوية الترابية لأن عناصر هذه المجموعة تتواجد بشكل كبير في صخور القشرة الأرضية.
-
"مجموعة البورون" (3A): وهي سلسلة العناصر الكيميائية الموجودة في المجموعة الثالثة عشر في الجدول الدوري والتي تحتوي على عنصر البورون. تميل لفقد ثلاثة إلكترونات وتكوين أيونات ثلاثية موجبة الشحنة.
-
"مجموعة الكربون" (4A): وهي سلسلة العناصر الكيميائية الموجودة في المجموعة الرابعة عشر في الجدول الدوري والتي تحتوي على عنصر الكربون. تميل عناصر هذه المجموعة إلى تكوين حالة تأكسد +4. تحتوي هذه المجموعة على عناصر فلزية ولا فلزية وأشباه فلزات أيضاً. الكربون عنصر لا فلزي.
-
"مجموعة النيتروجين" (5A): وهي سلسلة العناصر الكيميائية الموجودة في المجموعة الخامسة عشر في الجدول الدوري. تحتوي هذه المجموعة على عنصر البزموث وهو العنصر الفلزي الوحيد في هذه المجموعة، والزرنيخ والأنتيمون من أشباه الفلزات، أما النيتروجين والفوسفور فهم من اللافلزات. وتتراوح أعداد تأكسد مجموعة النيتروجين ما بين -3 إلى +5.
-
"مجموعة الأكسجين" (6A): وهي سلسلة العناصر الكيميائية الموجودة في المجموعة السادسة عشر في الجدول الدوري. وتضم عدة عناصر لا فلزية وأشباه فلزات منها: الأكسجين والكبريت. ويعد عنصري الأكسجين والكبريت عناصر لا فلزية. تتراوح أعداد التأكسد لهذه المجموعة ما بين -3 إلى +6.
-
"مجموعة الهالوجينات" (7A): هي سلسلة العناصر الكيميائية الموجودة في المجموعة السابعة عشر في الجدول الدوري. وتضم كلاً من العناصر التالية: (الفلور و الكلور و البروم واليود والاستاتين). وجميع العناصر فيها لا فلزات قوية، وتتميز مجموعة الهالوجينات بقدرتها العالية على التفاعل، ويعد الفلور العنصر الأكثر فعالية بينهم. وتعتبر عوامل مؤكسدة جيداً وتتفاعل بشدة مع الفلزات.
-
"مجموعة الغازات النبيلة" (8A): هي سلسلة العناصر الكيميائية الموجودة في المجموعة الثامنة عشر والأخيرة في الجدول الدوري في أقصى يمين الجدول. وتضم العناصر التالية: (هيليوم، نيون، أرجون، كريبتون، زينون، ورادون). وهذه العناصر خاملة كيميائياً ولا تتفاعل مع العناصر الأخرى إلا عند توفر طاقة عالية جداً تكفي لتأيين الكترونات مدارها الأخير. وسميت بهذا الاسم نسبة إلى طبيعتها الخاملة.
العناصر الانتقالية في الجدول الدوري
العناصر الانتقالية هي سلسلة العناصر التي تكون في ذرتها الفلك d غير مكتمل، وعددهم 40 عنصر متواجدين في 8 مجموعات موزعين في 10 أعمدة. تتواجد العناصر الانتقالية في منتصف الجدول الدوري أي بمعنى آخر يبدأ تواجدها في المجموعة 3B وتنتهي بالمجموعة 2B، تميز هذه العناصر بتكوين مركبات ملونة، ويكون لها أكثر من رقم تأكسد، وجميعها صلبة على درجة حرارة الغرفة باستثناء الزئبق فهو سائل. ومن الأمثلة الشهيرة على العناصر الانتقالية: التيتانيوم، الحديد، النحاس، الذهب، الفضة، البلاتين.
ملاحظة/ عناصر المجموعة 2B (عناصر مجموعة الزنك Zn) تعتبر عناصر انتقالية تجاوزاً؛ وذلك لأن الفلك d في ذرات عناصرها يكون مكتمل بالالكترونات.
ما هي اللانثانيدات والأكتنيدات "العناصر الانتقالية الداخلية"؟
-
اللانثانيدات: هي سلسلة من العناصر الأرضية النادرة وتبدأ أعدادها الذرية من 58 إلى 71، سميت بهذا الاسم نسبة إلى عنصر اللانثانوم (La) رغم أن بعض العلماء لا يصنفونه من ضمنها. عناصر مجموعة اللانثانيدات يكون فيها الفلك F مكتمل جزئياً أو كلياً بالإلكترونات.
-
الأكتينيدات: تتكون من 15 عنصر تبدأ بعنصر الأكتينيوم (Ac) إلى عنصر اللورنسيوم (Lr) بأعداد ذرية تبدأ من 89 إلى 103. عناصر مجموعة الأكتنيدات لا تتواجد في الطبيعة لأن لها أعداد ذرية كبيرة وعمر النصف لها صغير باستثناء اليورانيوم، والثوريوم، والبروتواكتينيوم.
من الجدير بالذكر أن موقع مجموعتي اللانثانيدات والأكتنيدات في الجدول الدوري هو أسفل الجدول الدوري؛ وذلك لأن خواصهما لا تتفق مع خواص العناصر الانتقالية.
في الختام، نكتشف أن الجدول الدوري يمثل بالفعل خارطة لفهم أسس الكيمياء والعناصر الكيميائية. فهو ليس مجرد ترتيب عشوائي، بل هو المفتاح الذي من خلاله نستطيع فهم التفاعلات الكيميائية بطريقة منظمة. نعلمك يا صديقي أن الجدول الدوري ما زال يشهد إضافات جديدة من العناصر، وما زال العلماء يبحثون عن عناصر كيميائية جديدة في عالمنا لإضافتها إلى الجدوَل الدوري.


 من الإبتسامة إلى التنفس: ما دور العضلات في حياتنا؟
من الإبتسامة إلى التنفس: ما دور العضلات في حياتنا؟
 إصابات الملاعب الشائعة وطرق التعامل معها | دليل شامل لمحبي الرياضة
إصابات الملاعب الشائعة وطرق التعامل معها | دليل شامل لمحبي الرياضة
